Химические и электрохимические методы обработки деталей.Электрохимическое окрашивание металлических деталей
Содержание.
- Общие сведения
- Нанесение металлических покрытий на неметаллические материалы
- Изготовление матриц и литейных форм из меди
- Обезжиривание внешней поверхности деталей
- Электрохимическое полирование поверхностей металлических деталей
- Электрохимическое окрашивание металлических деталей
- Декоративная отделка деталей из алюминия и его сплавов
- Химическое фрезерование металлов
- Химическое полирование металлов
- Нанесение надписей и рисунков на оргстекло методом травления
Для электрохимического окрашивания металлических деталей из стали, латуни и меди необходимо собрать гальваническую ванну и электрическую схему (рис. 4).
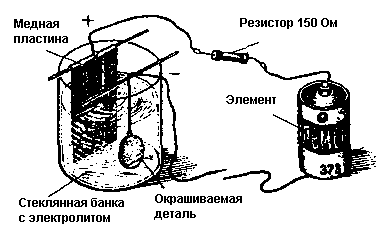
Рис. 4. Простейшая гальваническая ванна для окрашивания деталей
Электрод, подключенный к <плюсу>, делают из листовой меди. <Минус> подключают к окрашиваемой детали. Необходимо следить, чтобы детали не касались медной пластинки. В банку запивают специальный электролит и замыкают электрическую цепь. Через 2-3 мин начнется окрашивание. Сначала деталь станет коричневой, потом фиолетовой и т. д. Цвет зависит от времени: 2 мин - коричневый; 3 мин - фиолетовый; 3-5 мин - синий; 5-6 мин - голубой; 8-12 мин - желтый; 12-13 мин - оранжевый; 13-15 мин - красный; 17-21 мин - зеленый.
На 1 л электролита необходимо:
- медного купороса - 60 г;
- сахара-рафинада - 90 г;
- едкого натра - 45 г.
Приготавливается электролит в строгой последовательности: растворяется купорос в 200-300 мл воды, в него добавляется сахар. Отдельно в 250 мл воды растворяется едкий натрий. К нему небольшими порциями, при постоянном помешивании, подливается раствор медного купороса с сахаром. Затем добавляется вода, чтобы получился 1 л раствора.
При работе с едким натром, также как и с кислотами, надо соблюдать осторожность. Чтобы цвета были более контрастными, в готовый электролит добавляется 20 г безводной соли углекислого натрия. После окрашивания деталь промывают водой, сушат и покрывают бесцветным лаком.


